医械研发早期、成品如何开展生物相容性评价?
医疗器械风险管理是保证医疗器械安全有效的一项重要质量管理活动,贯穿于从设计开发到临床应用的医疗器械全生命周期。生物相容性风险作为医疗器械风险管理的一个重要方面,也是贯穿其始终的。对于直接或间接接触人体的医疗器械来说,良好的生物相容性是其临床安全有效应用的先决条件,是对其整体进行受益-风险评估的基础。
一、产品研发早期的生物相容性评价
在医疗器械的早期研发阶段,生物相容性评价主要针对原材料、生产工艺参数、加工助剂的筛选。对于医疗器械原材料的选择,主要考虑其是否满足医疗器械的设计输入。而原材料种类一旦选定,接下来的问题就是需要确认外购的原材料级别或者自制原材料质量是否适合用于生产预期设计的医疗器械。目前对于医用级材料或植入级材料尚无确切的定义。有的材料供应商对自己的材料有着相应级别的区分,以用作不信用途。虽然最终的安全性责任是由医疗器械制造商承担的,但医疗器械制造商在选择材料时仍需考虑供应商给出的建议。在筛选不同的材料或材料级别时,可以运用生物相容性评价的方式。此阶段的生物相容性需结合所能收集到的各种材料信息,如供应商提供的材料安全数据单(MSDS)、主文档(MAF)登记信息[4]、材料在已上市器械中的应用史等,但这些信息对于材料的筛选可能并不充分,还需通过化学表征对原材料的杂质进行分析,或者一些短期的、体外的生物学试验来进行验证。对于不同种类的加工助剂,不仅需要考虑其功能性,还要考虑其是否引入毒性物质,以及是否容易在后续工序中去除。而对干加工助剂残留量可接受性的确认,也会用到生物相容性评价方法,一般是采用对残留助剂的化学表征和毒理学评价相结合的方式。
二、终产品的生物相容性评价
对于已设计定型并在完善的质量管理体系下生产的医疗器械终产品,若其预期与人体直接或间接接触,则在其进行人体临床应用或临床试验之前,需对其进行充分、完整的生物相容性评价。终产品的生物相容性评价需要首先了解产品相关的化学组成,如原材料加工助剂、工艺中可能引入的污染物、可能生成的材料降解产物等,甚至需要考虑原材料本身制造过程引入的杂质(可以从原材料供应商处获取相关信息)在此基础上还可对终产品进行材料表征和可沥滤物分析以进一步验证其组成成分和杂质水平。建立在对产品化学组成和杂质水平充分了解基础上的生物相容性评价才更加可靠。
1、生物相容性评价路径
生物相容性评价有两种路径:整体评价路径和终点评路径(如下图示)
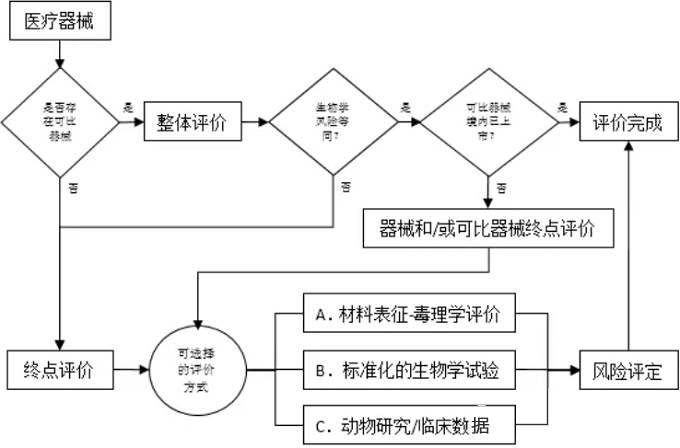
(1)整体评价路径
此种评价路径不需要选择评价终点,因为是对器械整体生物学风险的评估,但前提是所评价的终产品存在可比器械。可比器械为已在境内上市的器械或生物相容性评价证据链完整的器械,一般为本企业器标才具有可比性。可比器械如果与待评价器械在任何可能与生物学风险相关的方面(如材料配方和来源、生产工艺和灭菌工艺、物理状态、表面结构、初包装料,以及与人体的接触等)均相同,则可直接得出产品生物学风险等同的结论。若有任何细微差别,可对差别进行相关的对比分析并补充评价,以支持相关差异带来的额外生物学风险可接受。例如,其中某一种原材料的来源不同,可根据其接触途径等,必要开展适度的化学表征对其进行对比分析,证明是否产主额外的生物学风险。若可比器械为已在境内上市的医疗器械,则生物相容性评价完成;若可比器械未境内上市,则需针对各个评价终点确认可比器械的物相容性评价证据链是否完整,不完整的补充进行生物相容性评价。
(2)终点评价路径
如果所评价的终产品不存在可比器械,则需要步入点评价路径,即针对各个评价终点进行评价。一般可参照GB18666.1(ISO10993-1)中的评价终点阵图,根据终产品与人体接触的途径和时间确定需事平价的终点,如细胞毒性等。一些器械有对应的国家标准或行业标准,可参考相关标准进行选择。终点定后,不同的终点可以选择不同的评价方式。一般有下列三种评价方式可供选择:
A.材料表征-毒理学评价
材料表征-毒理学评价即参照GB/T16886.18(IS10993-18)进行材料化学表征,参照GB/688617(S010993-17)进行毒理学评价。1种方式一般适用于评价系统性的毒性终点,如全身生、遗传毒性、生殖毒性、致癌性。当生物学试验的不确定度很高时,可以考虑采用材料表征-毒理学课价的方式作为补充,但这种方式一般不用于评价细毒性、致敏、植入后局部反应、血液相容性等终点。毒理学问值(TTC)评价方法[5]也属于此种方式。批种方式除了用于部分终点的评价,还用于医疗器中具有一定毒性的加工助剂残留量的可接受性评价如有机溶剂、交联剂残留量,也可用于评估当器械原材料或加工助剂的来源或技术条件、产品某种次成分、生产工艺或灭参数、初包装材料等发生改时是否引入新的生物学风险,以及新的生物学风险是否可以接受。
B. 标准化的生物学试验
标准化的生物学试验采用终产品或有代表性的样品作为试验材料。无法直接试验的,通常用其浸提液进行式验。漫提的原则是尽可能与临床建立联系,在标的漫提条件中尽可能选择更苛刻的条件,以获得更的安全系数,如在材料不发生变化的情况下选择提能力更强的漫提介质、更高的漫提温度、更高的漫比例、更长的浸提时间等,但有时两种漫提条件之间目比并不存在绝对的严苛性。剂量选择也是在可行和尽可能大的安全系数之间的平衡。对于多次使用的器械还需要考虑生物学反应的积累效应。需要确认物学试验的样品能够代表最差状态,如货架储存时的考虑。对于观察局部反应的试验如植入试验、刺式验等,样品制备时还需要考虑表面结构的影响。更于结果的分析,生物学试验还需考虑是否设置照,如阴性对照、阳性对照等。需注意的是,对于戒组合产品,生物学试验结果可能会受到干扰,需要考虑是否将终产品和不含药部分分别进行评价。然,试验的质量控制也是非常重要的方面。
C. 动物研究/临床数据
一般所说的动物研究指的是模拟临床使用途径的原动物试验,主要用于医疗器械临床前可行性、有交生、安全性研究的目的。虽然其并不能充分识别生物学风险,但在一些特殊情形中也可以起到补充生物容性评价的作用。例如,当血栓形成试验中出现血平级较高的情况,可结合动物研究中的血栓形成数对结果的可接受性进行综合评价。还有对于带有药除层的球囊扩张导管评价药物的亚慢性毒性时也可合动物研究中的数据进行观察。但是,如果用动物究方式代替部分生物学试验来评价医疗器械的生物容性,则需考虑动物研究是否符合GB/16886(ISO 10993)系列标准对于相生物学试的观察指标、观时间点、动物数量、样品数量等具本要求。
临床数据虽然是最接近医疗器械真实应用安全性、效性的数据,但由于其观测方式的局限性以及其他就因素等条件所限,对于生物学风险的识别可能并不教感,因此临床数据一般不能直接用于生物相容性价,但可作为产品生物相容性评价的有益补充,如,对于某些生物学试验结果的临床可接受性评估有重要参考意义。
以上三种评价方式可以互相补充,对生物相容性评是供完整证据链。如果评价数据为文献或历史数据需要考虑适用性和数据质量等问题。
以上两条评价路径也可结合起来,如部分终点采用比器械数据,部分终点采用待评价器械数据。
2. 生物相容性评价结果的接受准则
主物相容性评价的结果并不能单独依据生物学试验数据讨论是否可以接受。医疗器械的生物相容性是否可接受是基于对终产品的受益和风险进行综合分析而判断的,因此需结合医疗器械的各项非临床和临研究数据以及其相关产品的临床应用信息。需要注的是,并不是所有的生物学反应都是不良的,或是期望的,有些反应是材料或其降解产物,结合特定的里作用(如生物力学作用)来激发宿主做出的适
三、持续进行的生物相容性评价
由于医疗器械的生物相容性评价贯穿于产品全生命周期,因此在产品上市后,仍然需持续关注其生物相容性。例如产品在运输、储存过程中的变化是否引起其生物相容性的改变。例如对于持久植入的器械,其远期的生物相容性信息如何在上市后评价中收集。例如原材料和加工助剂的来源和技术条件、产品配方、生产工艺、初包装、灭菌、适用范围等的变化是否引入新的生物学风险,如果引入则需补充进行生物相容性评价。








